刘定斌教授研究方向为利用先进的分离富集技术助力肿瘤标志物筛选;发展高灵敏、高特异性的肿瘤检测探针;建立面向临床转化的体外诊断新方法,刘定斌教授在Proc. Natl. Acad. Sci. USA., Nat. Commun., Sci.Adv., J.Am.Chem.Soc., Angew. Chem. Int. Ed.等国际知名刊物上发表论文 100 余篇,论文他引6600 余次;已获授权专利十余项,并实现其中多项专利的成果转化。先后获得国家级青年人才计划、科技部国家重点研发计划、国家基金委杰出青年基金和面上项目、军委后勤保障部重点项目等资助。在此,我们汇总了刘教授团队的代表性论文与大家一起分享,内容如下,Sci. Adv.:可逆两性离子配位能够从生物体液中快速、高产、高纯度地分离细胞外囊泡

细胞外囊泡(EV)是磷脂双层封闭结构,大小从30 nm到几微米不等,携带宿主细胞的特定蛋白质、核酸和小分子代谢物。EV经常在各种生物流体中被发现,如血清、尿液、唾液和眼泪,它们可以指示多种疾病的存在、发展和治疗反应。因此,EV已被公认为最有前景的液体活检生物标志物之一。然而,由于EV在生物流体中的浓度低,尺寸和成分的异质性程度高,EV的检测仍然是一个技术挑战。此外,纳米级脂蛋白和无细胞核酸等高丰度污染物经常共存于生物流体中,干扰EV检测,从而降低分析灵敏度和准确性。目前,由于缺乏高产量和高纯度的分离方法,EV的研究和部署受到严重阻碍。
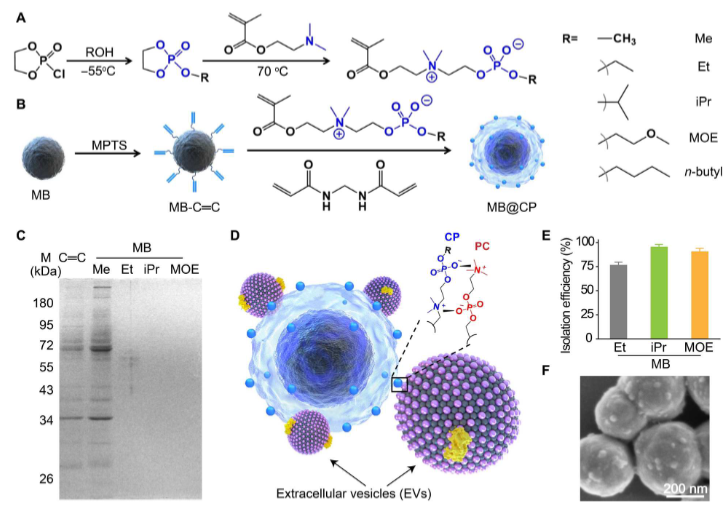
在这项研究中,南开大学刘定斌教授等人报告了一种可逆的两性离子配位策略,可以快速从不同的生物流体中分离出EV,突破了EV研究的长期困境,即同时以高产率和纯度从真实样品中捕获EV。该策略基于EV膜上的磷脂酰胆碱(PC)和锚定在磁珠(MB)上的“PC反向”磷酸胆碱(CP)之间的特定多价相互作用。PC是磷脂中含量最丰富的头基,是EV的基本成分。因此,预计PC-CP相互作用将捕获除非EV对应物之外的所有EV。此外,CP是一种具有防污作用的两性离子部分,它最大限度地减少了生物污染物在珠粒上的非特异性吸附。此外,通过稍微改变环境温度,可以可逆地调节PC-CP配位,这使得EV可以从珠子中瞬时释放出来,用于下游研究。这项创新技术的潜在应用通过与蛋白质组学相结合来鉴定癌症生物标志物,并进一步将EVs从各种临床相关的生物流体中分离出来。与金标准UC和其他传统方法相比,这种基于可逆两性离子配位的平台能够以显著更快的处理速度、产量和纯度实现EV分离,这意味着临床转化的巨大前景。
 细胞外囊泡(EV)是磷脂双层封闭结构,大小从30 nm到几微米不等,携带宿主细胞的特定蛋白质、核酸和小分子代谢物。EV经常在各种生物流体中被发现,如血清、尿液、唾液和眼泪,它们可以指示多种疾病的存在、发展和治疗反应。因此,EV已被公认为最有前景的液体活检生物标志物之一。然而,由于EV在生物流体中的浓度低,尺寸和成分的异质性程度高,EV的检测仍然是一个技术挑战。此外,纳米级脂蛋白和无细胞核酸等高丰度污染物经常共存于生物流体中,干扰EV检测,从而降低分析灵敏度和准确性。目前,由于缺乏高产量和高纯度的分离方法,EV的研究和部署受到严重阻碍。
细胞外囊泡(EV)是磷脂双层封闭结构,大小从30 nm到几微米不等,携带宿主细胞的特定蛋白质、核酸和小分子代谢物。EV经常在各种生物流体中被发现,如血清、尿液、唾液和眼泪,它们可以指示多种疾病的存在、发展和治疗反应。因此,EV已被公认为最有前景的液体活检生物标志物之一。然而,由于EV在生物流体中的浓度低,尺寸和成分的异质性程度高,EV的检测仍然是一个技术挑战。此外,纳米级脂蛋白和无细胞核酸等高丰度污染物经常共存于生物流体中,干扰EV检测,从而降低分析灵敏度和准确性。目前,由于缺乏高产量和高纯度的分离方法,EV的研究和部署受到严重阻碍。 在这项研究中,南开大学刘定斌教授等人报告了一种可逆的两性离子配位策略,可以快速从不同的生物流体中分离出EV,突破了EV研究的长期困境,即同时以高产率和纯度从真实样品中捕获EV。该策略基于EV膜上的磷脂酰胆碱(PC)和锚定在磁珠(MB)上的“PC反向”磷酸胆碱(CP)之间的特定多价相互作用。PC是磷脂中含量最丰富的头基,是EV的基本成分。因此,预计PC-CP相互作用将捕获除非EV对应物之外的所有EV。此外,CP是一种具有防污作用的两性离子部分,它最大限度地减少了生物污染物在珠粒上的非特异性吸附。此外,通过稍微改变环境温度,可以可逆地调节PC-CP配位,这使得EV可以从珠子中瞬时释放出来,用于下游研究。这项创新技术的潜在应用通过与蛋白质组学相结合来鉴定癌症生物标志物,并进一步将EVs从各种临床相关的生物流体中分离出来。与金标准UC和其他传统方法相比,这种基于可逆两性离子配位的平台能够以显著更快的处理速度、产量和纯度实现EV分离,这意味着临床转化的巨大前景。
在这项研究中,南开大学刘定斌教授等人报告了一种可逆的两性离子配位策略,可以快速从不同的生物流体中分离出EV,突破了EV研究的长期困境,即同时以高产率和纯度从真实样品中捕获EV。该策略基于EV膜上的磷脂酰胆碱(PC)和锚定在磁珠(MB)上的“PC反向”磷酸胆碱(CP)之间的特定多价相互作用。PC是磷脂中含量最丰富的头基,是EV的基本成分。因此,预计PC-CP相互作用将捕获除非EV对应物之外的所有EV。此外,CP是一种具有防污作用的两性离子部分,它最大限度地减少了生物污染物在珠粒上的非特异性吸附。此外,通过稍微改变环境温度,可以可逆地调节PC-CP配位,这使得EV可以从珠子中瞬时释放出来,用于下游研究。这项创新技术的潜在应用通过与蛋白质组学相结合来鉴定癌症生物标志物,并进一步将EVs从各种临床相关的生物流体中分离出来。与金标准UC和其他传统方法相比,这种基于可逆两性离子配位的平台能够以显著更快的处理速度、产量和纯度实现EV分离,这意味着临床转化的巨大前景。



